گاز چیست ؟
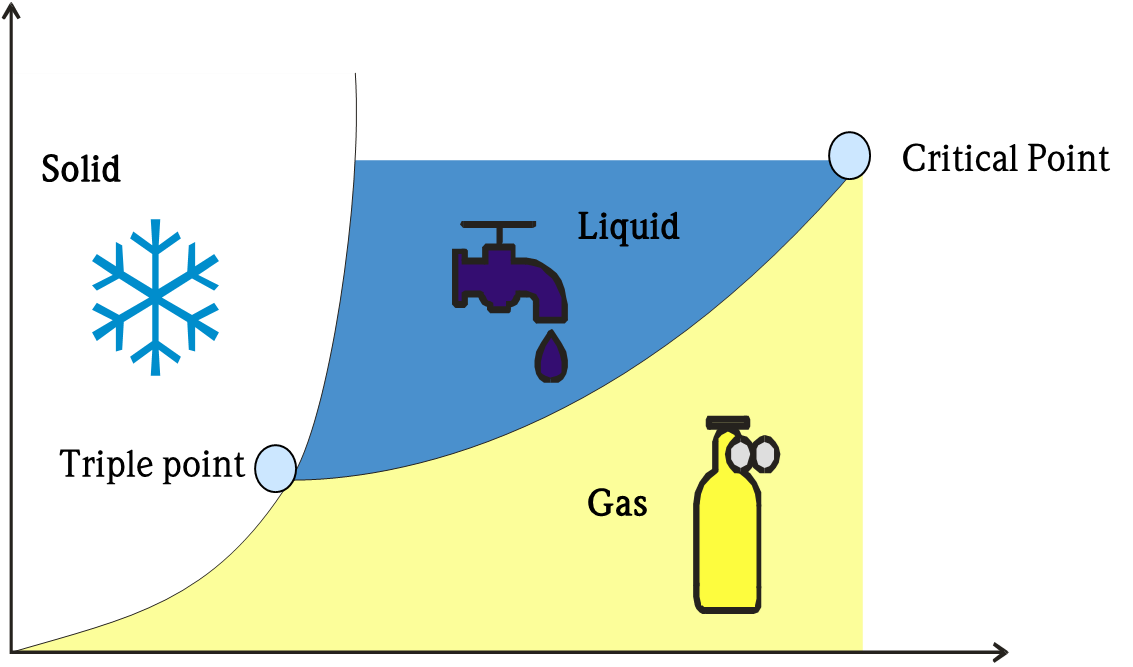
منحنی فوق , منحنی تعادل آب نیست
هر سیالی از جمله گازها میتوانند در 3 فاز ممکن ظاهر شوند . مایعات در نقطه جوش خودشان تغییر به گاز پیدا میکنند و در در نقطه انجماد خودشان تغغیر به فاز جامد میدهند و هر یک از این انتقالها وابسته به دما و فشار است .
نقطه سه گانه یا Triple Point :
در فیزیک نقطه سه گانه یک ماده دما و فشاری است که 3 فاز گاز مایع و جامد ان ماده میتوانند در تعادل ترمودینامیکی باشند .برای مثال نقطه سه گانه جیوه در دمای 38.8344 – سانتیگراد و فشار0.5 میلی پاسگال است .
نقطه بحرانی یا Critical Point :
در فیزیک یک نقطه مهم نقطه خاتمه یک منحنی تعادل فاز است . در این نقطه دیگر فازهای یک ماده قابل تشخیص نیستند
مایع : حجم ثابت ولی شکل متغیر دارد 
جامد : حجم ثابت و شکل ثابت دارد .
گازها : نه حجم ثابت و نه شکل ثابت دارند
تعریف گاز
هر سیالی که مدل گاز را در دمای 20 درجه سانتیگراد و فشار یک بار داشته باشد گاز نامیده می شود .
مولکولهای گاز بر خلاف مایعات و جامدات به یکدیگر متصل نیستند و حرکت آزادانه دارند
گازها هر حجمی را در صورتیکه تحت تراکم و یا انبساط قرارگیرند اشغال می کنند
بنابراین گازها تراکم پذیر هستند .
گاز ایده ال (Ideal gas)/قانون بویل

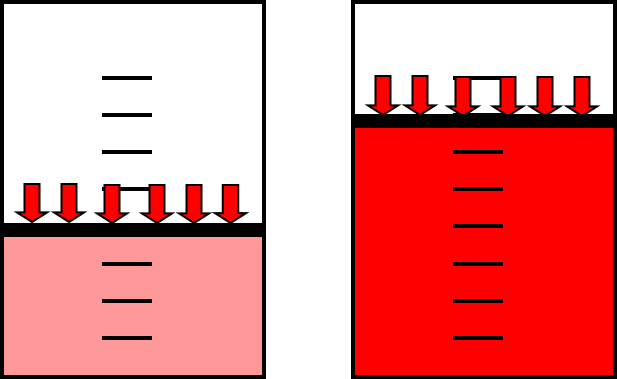
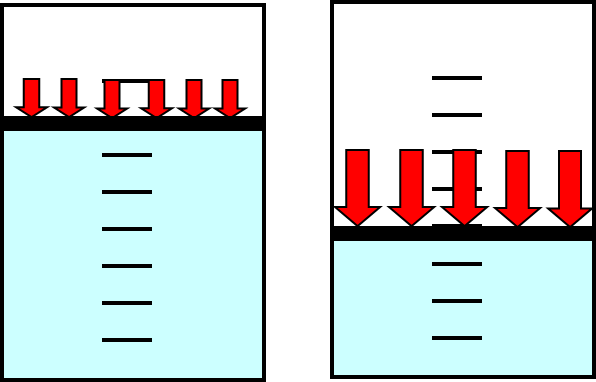
• در سال 1662 رابرت بویل ثابت كرد كه در دمای ثابت حجم گاز رابطه معکوس با فشار آن دارد
• بنابراین اگر گاز ها را در دمای ثابت قرار دهیم و فشار را بالا ببریم حجم گاز کاهش می یابد و اگر فشار را کم کنیم حجم آن افزایش می یابد.
• قاون بویل که صرفا برای گازهای ایده ال قابل اعمال میباشد در سیستم های فلو میترینگ بسیار حائز اهمیت میباشد زیرا بدلیل افت فشار در سیستم پایپینگ و خود فلومیتر ,حجم گاز افزایش پیدا میکند
گاز ایده ال (Ideal gas)/قانون گیلوساک
 • در سال 1802 گیلوساک ثابت کرد در فشار ثابت حجم گاز با دمای آن (برحسب کلوین ) رابطه مستقم دارد
• در سال 1802 گیلوساک ثابت کرد در فشار ثابت حجم گاز با دمای آن (برحسب کلوین ) رابطه مستقم دارد
• اگر ظرفی را از گاز در فشار ثابت پرکنیم و آن را حرارت بدهیم حجم گاز اضافه میگردد
• یا اگر حجم گاز را ثابت نگه داریم و دمارا افزایش دهیم آنگاه فشارمطلق گاز افزایش می یابد و با کاهش دما , فشار مطلق گاز کاهش می یابد
محاسبه دبی جرمی :

• فلوی جرمی با حاصلضرب فلوی حجمی در دانسیته گاز در شرائط پروسه قابل محاسبه می باشد
• محاسبه فلوی حجمی به راحتی توسط فلو میترهای حجمی ماندد ورتکس و ..قابل اندازه گیری می باشد .
• مشخص نمودن دانسیته در شرائط پروسه آنقدر که به نظر میرسد آسان نیست .
به توضیحات بیتشر در مقاله های آتی دقت فرمائید.













-50x50.jpg)














نظر خود را بیان کنید